На сайте журнала Journal of Materials Chemistry C (IF=5,1) по результатам работы, выполненной совместно с коллегами из Московского государственного университета им. М.В. Ломоносова и Института синтетических полимерных материалов им. Н.С. Ениколопова РАН, , опубликована статья, соавторами которой является сотрудники Института: Е.Д.Толкачев (мнс, ЛОЭ), к.х.н. К.С. Мельникова-Беккер (снс, ЛОЭ), к.х.н. А.А. Сонина (снс, ЛОЭ), к.х.н. И.К. Шундрина (снс, ЛЭАСМ), д.ф.-м.н., проф. Е.Г. Багрянская (директор Института, Завлаб ЛМР), д.х.н. М.С. Казанцев (завлаб ЛОЭ) :
Highly photostable and emissive thienyl-containing tris(2,4,6-trichlorophenyl)methyl radicals
Egor D. Tolkachev, Christina S. Becker, Vasily A. Trukhanov, Nikita O. Dubinets, Mikhail B. Zuev, Alina A. Sonina, Inna K. Shundrina, Elena G. Bagryanskaya, Dmitry Yu. Paraschuk and Maxim S. Kazantsev
J. Mater. Chem. C, 2026, Advance Article
First Published: 16 Feb 2026
https://doi.org/10.1039/D5TC04519C
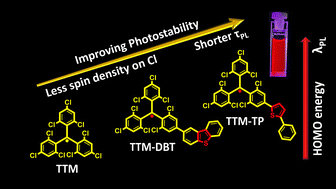
Ученые синтезировали и изучили новый класс люминесцентных органических радикалов на основе тритильной группы с тиофенсодержащими донорными фрагментами. Полученные соединения демонстрируют высокую фотостабильность, превышающую исходный незамещенный радикал более чем в тысячу раз, и эффективную люминесценцию в красной и ближней инфракрасной области.
Abstract
Luminescent organic radicals are among the most promising materials for spintronics, upconversion, red and near infrared (NIR) organic light-emitting diodes suffering from the spin-statistics limitations. However, the number of emissive radicals applied in electronic devices is limited, and their design principles are still under discussion. Here we designed, synthesized and studied a series of tris(2,4,6-trichlorophenyl)methyl (TTM) radicals with thiophene-based donors. The radicals were synthesized via cross-coupling reaction of a convenient monobromo-substituted TTM precursor followed by proton elimination and oxidation. Our DFT calculations and experimental data indicate that the HOMO energy of the donor strongly affects the radical emission properties. The radical with the highest optical gap demonstrated deep red electroluminescence and photoluminescence with a quantum yield of up to 12%. The photostability of radicals was found to increase dramatically with substitution, and, according to the proposed mechanistic picture, the spin density on chlorine atoms, and the energy and lifetime of the lowest excited state, D1, control the photodegradation rate. Our results not only extend the pool of the luminescence radicals but also provide clear physical and chemical insights into their fundamental structure–property relations and may serve as the basis for future molecular design of highly stable and emissive radicals.